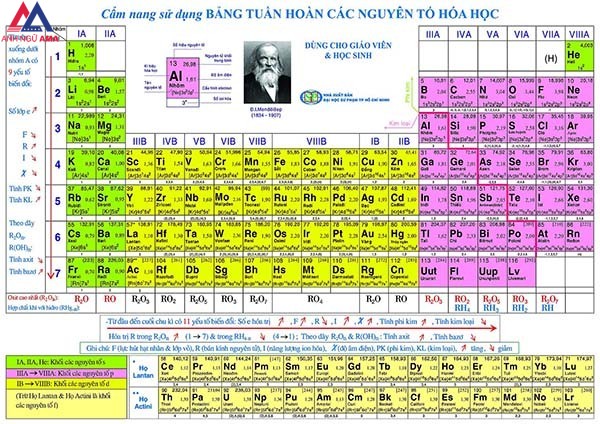
Trong Hoá Học, bảng tuần hoàn nguyên tố hoá học là vật cần thiết thiếu đối với mọi học sinh. Tuy nhiên, ko phải ai cũng hiểu rõ về bảng này và biết cách sử dụng như vậy nào. Đừng lo vì bài viết dưới đây công ty chúng tôi sẽ hỗ trợ cho các bạn tất cả rất nhiều thông tin cần thiết nhất.
Bảng tuần trả nguyên tố hóa học là gì?
Cấu tạo ra bảng tuần hoàn những nguyên tố hoá học
Ô nguyên tố
Chu kỳ
Nhóm nguyên tố
Có từng nào nguyên tố vào bảng tuần hoàn
Bảng tuần hoàn các nguyên tố chất hóa học được sắp xếp theo bề ngoài nào
Cách xem bảng tuần hoàn hóa học
Số nguyên tử
Nguyên tử khối trung bình
Độ âm điện
Cấu hình electron
Số oxi hoá
Tên nguyên tố
Ký hiệu hoá học
Hướng dẫn học thuộc bảng tuần hoàn Học theo phương pháp truyền thống
Mẹo học thuộc bảng tuần hoàn
Bảng tuần hoàn những nguyên tố chất hóa học tiếng Anh
Bảng tuần hoàn các nguyên tố hoá học tập còn mang tên gọi không giống là bảng tuần hoàn Mendeleev. Bảng này thể hiện những nguyên tố hoá học dựa trên cách bố trí số hiệu nguyên tử của chúng.
Bạn đang xem: Bảng tuần hoàn các nguyên tố hóa học: cách học và mẹo ghi nhớ
Nó được Dimitri Mendeleev sáng tạo và sử dụng rộng thoải mái vào năm 1869. Sau đó, bảng này được ứng dụng trong những công trình nghiên cứu khoa học. Phụ thuộc vào nó, con người hoàn toàn có thể dễ dàng đọc về sự quản lý của những nguyên tố và các quy hình thức hoá học tập khác. So với thời điểm mới ra mắt, bảng tuần trả hoá học sẽ được bổ sung thêm một số nguyên tố mới.
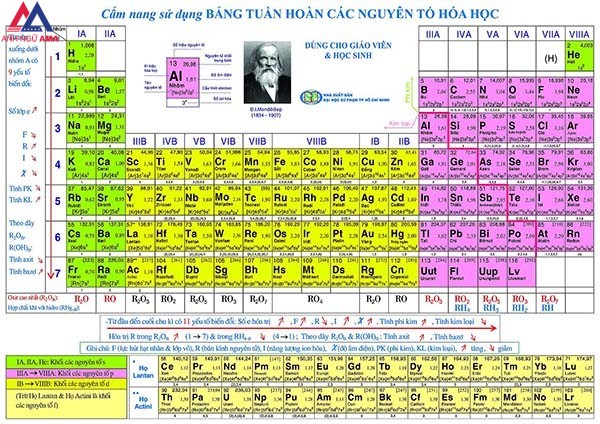
Cấu tạo thành bảng tuần hoàn những nguyên tố hoá học
Ô nguyên tố
Ô nguyên tố cung cấp thông tin gồm: cam kết hiệu hoá học, tên nguyên tố, số hiệu nguyên tử, nguyên tử khối của thành phần đó.
Trong đó, số hiệu nguyên tử tất cả số trị bởi số đơn vị điện tích hạt nhân và bằng số E vào nguyên tử. Số hiệu nguyên tử đồng thời chính là số lắp thêm tự của nguyên tố đó trong bảng tuần hoàn. Ví dụ: Số hiệu nguyên tử của Al là 13 mang đến biết: Al sống ô số 13, điện tích hạt nhân nguyên tử là 13+, gồm 13 electron vào nguyên tử Nhôm
Chu kỳ
Chu kỳ là 1 trong dãy các nguyên tố nhưng mà nguyên tử của chúng tất cả cùng số lớp electron với được xếp theo lắp thêm tự năng lượng điện hạt nhân tăng dần. Thông thường, chu kỳ có số thiết bị tự bằng số lớp electron.Bảng tuần trả hoá học có 7 chu kỳ, vào đó, những chu kỳ nhỏ dại là chu kỳ số 1,2,3, sót lại là những chu kỳ lớn.
Chu kỳ 1: tất cả 2 nguyên tố có H cùng HeChu kỳ 2: tất cả 8 thành phần Li, Be, B, C, N, O, F, Ne
Chu kỳ 3: gồm 8 yếu tố Na, Mg, Al, Si, P, S, Cl, Ar
Chu kỳ 4 và chu kỳ 5: Mỗi chu kỳ luân hồi có 18 nguyên tố, bắt đầu là một sắt kẽm kim loại kiềm và ngừng là một khí hiếm
Chu kỳ 6: bao gồm 32 nguyên tố, trường đoản cú Cs mang đến Rn
Chu kỳ 7: không hoàn thiện
Nhóm nguyên tố
Nhóm thành phần gồm những nguyên tố mà trong đó nguyên tử của chúng có cùng số electron phần bên ngoài cùng. Chúng gồm tính chất giống như nhau cùng được xếp theo thứ tự theo chiều tăng của điện tích hạt nhân. Số máy tự của group nguyên tố được tính bằng số electron lớp bên ngoài cùng của nguyên tử.Có 2 các loại nhóm yếu tắc là nhóm A và nhóm B. Vào đó:Nhóm A: Gồm những nguyên số s với p
Nhóm B: Gồm những nguyên tố d với f
Có bao nhiêu nguyên tố vào bảng tuần hoàn
Tính đến thời gian hiện tại, tổng cộng có 118 nguyên tố trong bảng tuần hoàn được xác thực, bao hàm từ thành phần 1 (Hydro) cho tới 118 (Oganesson).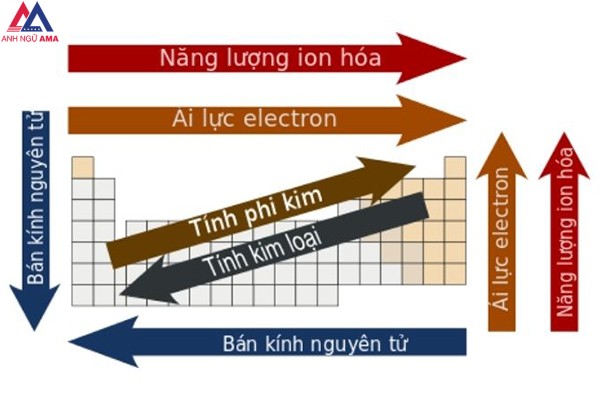
Trong tổng số 118 thành phần của thì bao gồm đến 98 nguyên tố mở ra trong từ bỏ nhiên, trăng tròn nguyên tố sót lại từ Ensteini đến Oganesson thường chỉ lộ diện ở các phép tổng hợp nhân tạo. Trong những 98 nguyên tố lộ diện trong tự nhiên và thoải mái thì có 84 yếu tố nguyên thuỷ – tức là chúng sẽ được mở ra trước khi Trái khu đất được hình thành. 14 nguyên tố còn lại chỉ xuất hiện thêm trong những chuỗi phân rã của các nguyên tố nguyên thuỷ đó. Ở dạng tinh khiết, không nguyên tố nào nặng hơn Einsteini (99).
Bảng tuần hoàn những nguyên tố chất hóa học được sắp xếp theo bề ngoài nào
Các yếu tố trong bảng tuần hoàn chất hóa học được bố trí dựa trên các nguyên tắc sau:Nguyên tắc 1: những nguyên tố hóa học.i.được bố trí theo chiều tăng dần.i.của năng lượng điện hạt nhân
Cách coi bảng tuần trả hóa học
Số nguyên tử
Số nguyên tử hay còn gọi là số proton của một yếu tắc hoá học. Số proton này được search thấy trong hạt nhân của nguyên tử đó, giúp xác định nguyên tố hoá học tập đó. Số nguyên tử ngay số E trong một nguyên tử trung hoà về điện.Nguyên tử khối trung bình
Đa phần các nguyên tố hoá học hầu hết là lếu hợp của rất nhiều đồng vị cùng với tỷ lệ tỷ lệ số nguyên tử xác định khác nhau. Vị vậy đề xuất nguyên tử khối của các nguyên tố có nhiều đồng vị hay là vừa phải khối của những đồng vị có tính đến tỷ lệ phần trăm số nguyên tử tương ứng.
Độ âm điện
Độ âm điện là năng lực hút electron của một nguyên tử trong số liên kết hoá học. Độ âm năng lượng điện của nguyên tử nhân tố càng nhỏ tuổi thì tính phi kim càng yếu và ngược lại.Cấu hình electron
Cấu hình electron của nguyên tử cho biết sự phân bố các electron trong nguyên tử kia ở những trạng thái năng lượng khác nhau ở nghỉ ngơi vùng hiện diện của chúng.Số oxi hoá
Số oxi hoá là số của một nguyên tử hoặc một đội nhóm nguyên tử, cho biết số electron trao đổi lúc 1 chất bị khử hoặc bị oxi hoá trong một phân tử.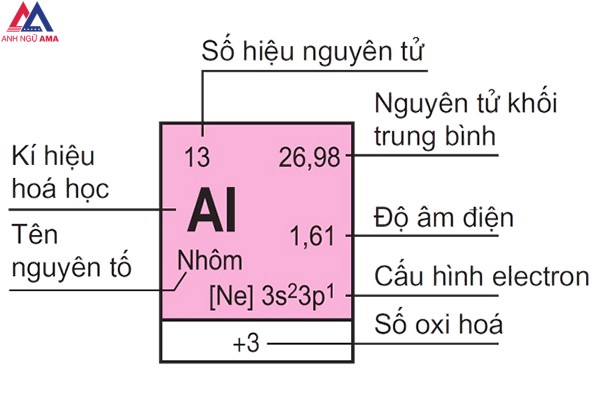
(adsbygoogle = window.adsbygoogle || <>).push();
Tên nguyên tố
Tên nguyên tố đại diện thay mặt cho chất hoá học kia ở dạng tinh khiết, bao gồm một kiểu nguyên tử, được rõ ràng bởi số hiệu nguyên tửKý hiệu hoá học
Ký hiệu hoá học là tên gọi viết tắt của nhân tố hoá học đó, thường bao gồm từ 1 mang đến 2 vần âm trong bảng chữ cái Latinh, trong số đó chữ thứ nhất viết hoa.Hướng dẫn học tập thuộc bảng tuần hoàn
Học theo phương pháp truyền thống
Ở cách thức này, các bạn sẽ nhận biết những thành phần yếu tắc theo 7 đầu mục mà chúng tôi vừa liệt kê ngơi nghỉ mục trên. Theo đó, mỗi ngày, chúng ta nên chia ra học từ 3-5 thành phần để dễ dàng ghi ghi nhớ hơn. Để dễ dàng hơn cho bài toán học, bạn nên dán bảng tuần trả ở mọi các quanh vùng thường xuyên đi qua. Lúc đó, bạn cũng có thể nhìn thấy và thuận lợi học thuộc mọi nguyên tố kia trong ngày.Mẹo học tập thuộc bảng tuần hoàn
Vì bảng tuần hoàn các nguyên tố có nhiều thông tin nên có một vài mẹo khiến cho bạn học ở trong bảng tuần hoàn hối hả hơn như sau:Mẹo 1: học thuộc câu nói giành riêng cho 16 nguyên tố vận động hoá học của kim loại“ lúc nào cần may áo gần cạnh sắt nhớ sang phố hỏi siêu thị Á Phi Âu “ tương xứng lần lượt với những nguyên tố K, Na, Ca, Mg, Al, Zn, Fe, N, S, P, H, Cu, Hg, Ag, Pt, Au. Mẹo 2: học thuộc 6 nguyên tố team IA“Lâu nay không từ tốn coi phim” khớp ứng lần lượt với những nguyên tố Li, Na, K, Rb, Cs, Pr
Mẹo 3: bài ca hoá trịĐây là một trong bài ca được mách nhau từ nhiều năm để giúp các bạn học trực thuộc số hoá trị của từng nguyên tố.

Bảng tuần hoàn những nguyên tố chất hóa học tiếng Anh
Khi có tác dụng quen với lịch trình hóa học, các em học sinh cần phải biết đến bảng tuần trả hóa học và ghi lưu giữ chúng. Để giúp các bạn dễ dàng rộng trong quá trình học, q6.edu.vn đem lại cho các bạn bài viết có những mẹo ghi ghi nhớ bảng tuần trả một cách chi tiết và biện pháp đọc, những định nghĩa cơ phiên bản để làm bài xích một cách chủ yếu xác.
1. Bảng tuần hoàn hóa học là gì?
Bảng tuần hoàn chất hóa học hay nói một cách khác là bảng tuần trả Mendeleev, là phương pháp dạng bảng hiển thị lên các nguyên tố hóa học phát minh vào năm 1869 vị nhà chất hóa học Dimitri Mendeleev bạn Nga.
Bảng tuần hoàn hóa học biểu hiện nguyên tố hóa học theo cách bố trí số hiệu nguyên tử của nguyên tố, thông số kỹ thuật electron và quy giải pháp tuần hoàn khác. Giá trị của bảng tuần hoàn hóa học là rất có thể tính toán tính chất hóa học tập của một nguyên tố dựa trên vị trí của nó.
Bảng tuần trả hóa học tương đối đầy đủ nhất sẽ được tổng thích hợp cho chúng ta học sinh nắm rõ. Bởi vậy hãy theo dõi thật kỹ càng nhé!
2. Cấu trúc của bảng tuần hoàn
2.1. Ô nguyên tố
Ô nguyên tố biểu hiện ra cho chúng ta biết những số hiệu nguyên tử, tên nguyên tố, cam kết hiệu hóa học, nguyên tử khối của yếu tắc đó. Số hiệu nguyên tử có số trị bằng số đơn vị chức năng của năng lượng điện hạt nhân và bằng số electron trong nguyên tử. Số hiệu nguyên tử là số đồ vật tự của nguyên tố đó ở trong bảng tuần hoàn.
Ví dụ: Số hiệu nguyên tử của Magie là 12 cho thấy rằng số đơn vị chức năng điện tích hạt nhân là 12, Magie nghỉ ngơi ô số 12, có 12 electron vào nguyên tử Magie.
2.2. Chu kỳ
Chu kỳ được đọc là dãy các nguyên tố nhưng nguyên tử của chúng được xếp theo chiều điện tích hạt nhân tăng dần và bao gồm cùng số lớp electron.
Số lớp electron = STT của chu kỳ.
Bảng tuần hoàn hóa học gồm tất cả 7 chu kỳ, trong số ấy có các chu kỳ bé dại là chu kỳ 1, 2, 3, những chu kỳ to là 4, 5, 6, 7.
Chu kỳ 1: tất cả 2 nguyên tố là He cùng H, có 1 lớp electron trong nguyên tử. Điện tích phân tử nhân tăng tự H 1+ cho tới He 2+.
Chu kỳ 2: 8 nguyên tố từ Li đến Ne, tất cả 2 lớp electron trong nguyên tử. Điện tích phân tử nhân tăng từ bỏ Li 3+ tới Ne là 10+.
Chu kỳ 3: gồm 8 nguyên tố từ thành phần Na cho Ar, có 3 lớp electron trong nguyên tử cùng điện tích hạt nhân tăng từ na 11+ cho nguyên tố Ar là 18+.
Chu kỳ 4, chu kỳ 5: đối với cả 2 chu kỳ, mỗi chu kỳ đều có 18 nguyên tố, bắt đầu là kim loại kiềm K là 19+ cùng Rb là 37+, ngừng là một khí thảng hoặc Xe là 54+ và Kr là 36+.
Chu kỳ 6: ban đầu từ sắt kẽm kim loại kiềm Cs là 55+ và xong là khí thảng hoặc Rn là 86+. Bao gồm 32 nguyên tố,
Chu kỳ 7: chưa được hoàn thành.
2.3. Nhóm nguyên tố
Vậy bảng tuần hoàn hóa học tất cả bao nhiêu nguyên tố? và được chia thành các nhóm ráng nào?
Bảng tuần trả hóa học bao gồm 118 nguyên tố, gồm những nguyên tố từ là 1 (Hidro) mang lại 118 (Oganesson). Nhóm những nguyên tố nhưng nguyên tử có số electron lớp bên ngoài cùng bằng nhau và do tất cả tính chất tựa như nhau được xếp theo hướng tăng của điện tích hạt nhân nguyên tử.
Số lắp thêm tự của group nguyên tố ngay số electron lớp bên ngoài cùng của nguyên tử.
Xem thêm: Quê của hồ quang hiếu - tiểu sử ca sĩ hồ quang hiếu
Ta tạo thành 2 loại nhóm yếu tố là đội nguyên tố A cùng nhóm B:
Nhóm A: Gồm các nguyên tố p và s. Số team A bởi tổng số electron phần ngoài cùng.
Nhóm B: Gồm các nguyên tố f và d có thông số kỹ thuật electron nguyên tử thì tận thuộc sẽ làm việc dạng (n-1) dxnsy
+ nếu (x+y) = 3 -> 7 thì nguyên tố sẽ xét thuộc team (x+y)B.
+ nguyên tố thuộc team VIIIB giả dụ (x+y) = 8 -> 10.
+ yếu tắc thuộc team (x+y-10)B giả dụ (x+y) > 10 thì
3. Ý nghĩa bảng tuần trả hóa học
Dựa vào bảng tuần hoàn hóa học, ta rất có thể biết vị trí của nguyên tố và suy đoán ra đặc thù của yếu tắc và kết cấu nguyên tử.
Ví dụ: nhân tố A với số hiệu nguyên tử 17, thuộc nhóm VIIA, vào chu kì 3.
Nguyên tố A có số hiệu nguyên tử là 17, buộc phải điện tích phân tử nhân của nguyên tử A là 17+, nguyên tử A bao gồm 17 electron.
Nguyên tố A nhóm VIIA nên hoàn toàn có thể suy ra phần ngoài cùng bao gồm 7e, ngơi nghỉ chu kì 3 phải nguyên tử A tất cả 3 lớp electron.
Tính phi kim của yếu tố A yếu rộng nguyên tố phía trên nó thuộc nhóm (nguyên tố F bao gồm số hiệu nguyên tử 9), khỏe mạnh hơn nguyên tố trước nó trong cùng 1 chu kì (S có số hiệu 16) với nguyên tố đứng dưới nó trong thuộc nhóm (Br tất cả số hiệu nguyên tử 35). Vì ở chỗ gần cuối chu kì 3 phải nguyên tố A là 1 trong phi kim mạnh.
Bảng tuần hoàn hóa học giúp chúng ta biết cấu tạo nguyên tử của nguyên tố rất có thể suy ra địa chỉ và đặc thù nguyên tố ấy.
Ví dụ: yếu tố Y gồm điện tích phân tử nhân là 11+, lớp bên ngoài cùng có 1 electron, 3 lớp electron
Vì yếu tố Y tất cả điện tích phân tử nhân là 11+, 3 lớp electron và gồm 1e ở phần ngoài cùng, phải nguyên tố Y ngơi nghỉ chu kì 3, ô 11, team IA.
→ nguyên tố Y là kim loại vì nó ở đầu chu kỳ.
4. Bảng tuần hoàn hóa học Mendeleev
Bảng tuần trả hóa học rất đầy đủ còn theo luồng thông tin có sẵn đến tên gọi là bảng tuần hoàn hóa học Mendeleev.
Bảng nguyên tố hóa học lớp 8
Bước vào lịch trình Hóa học lớp 8, Bộ giáo dục và đào tạo và đào tạo và giảng dạy cho học viên tiếp xúc với một số vấn đề liên quan đến bảng tuần hoàn. Điều này góp học sinh có thể làm thân quen được điều căn bản, đọc được thực chất của vấn đề. Một vài điều mà học viên sẽ được tiếp cận là:
Nguyên tử
Nguyên tố hóa học
Bảng tuần hoàn chất hóa học lớp 9:
Với Hóa 9, học viên sẽ được mẫu nhìn khái quát về bảng tuần hoàn hóa học. Sơ lược 1 số kiến thức và kỹ năng về bảng tuần hoàn hóa học, bao gồm có:
Nguồn gốc
Nguyên tắc sắp đến xếp các nguyên tố
Cấu tạo
Sự chuyển đổi tính chất các nguyên tố
Ý nghĩa của bảng tuần hoàn

https://toanhoc.org/wp-content/uploads/2020/08/Bang-tuan-hoan-hoa-hoc-4.jpg
Alt: Lớp 9 bảng tuần trả hóa học
Bảng nguyên tố chất hóa học lớp 10:
Sau lúc đã được gia công quen với bảng tuần hoàn các nguyên tố chất hóa học thì lúc lên lớp 10, đòi hỏi học sinh yêu cầu nắm chắc kỹ năng và kiến thức thật chắc. Trong hóa học 10, bảng tuần hoàn hóa học chủ yếu chỉ đi sâu rộng về: xuất phát về sự vạc minh, hiệ tượng sắp xếp những nguyên tố, cấu trúc bảng tuần hoàn, bài luyện tập nâng cao, cơ bản.
5. Nguyên lý sắp xếp những nguyên tố vào bảng tuần hoàn
Trong bảng tuần trả hóa học, những nguyên tố sẽ được sắp xếp theo chiều tăng cao của điện tích hạt nhân nguyên tử.
6. Phương pháp đọc bảng tuần trả hóa học
Để học viên sử dụng bảng tuần trả một bí quyết dễ dàng, hãy xem bí quyết đọc bảng tuần trả hóa học dưới đây:
+ Số nguyên tử: Còn có tên gọi không giống là số proton của yếu tắc hóa học. Đây là số proton search thấy trong phân tử nhân của 1 nguyên tử. Là số năng lượng điện hạt nhân. Số nguyên tử giúp xác định được tốt nhất 1 nguyên tố hóa học.
+ Nguyên tử khối trung bình: Nguyên tử khối của những nguyên tố bao gồm đồng vị là số NTK trung bình của láo lếu hợp các đồng vị, tính cho tỷ lệ tỷ lệ số nguyên tử tương ứng.
+ Độ âm điện: Là tài năng hút electron của nguyên tử khi tạo liên kết hóa học. Lúc độ âm điện của nguyên tử nhân tố càng béo thì tính phi kim càng dạn dĩ và ngược lại
+ thông số kỹ thuật electron: cho thấy phân bố các electron trong lớp vỏ nguyên tử làm việc trạng thái năng lượng khác nhau.
+ Số oxi hóa: Số thoái hóa là số áp cho 1 hay nhóm nguyên tử. Nhờ tất cả số oxi hóa mà chúng ta nhận biết được số electron trao đổi khi một chất bị oxi hóa hoặc bị khử.
+ tên nguyên tố: là 1 trong những chất hóa học tinh khiết, gồm 1 kiểu nguyên tử, được sáng tỏ bởi số hiệu nguyên tử, là số lượng proton bao gồm trong phân tử nhân.
+ ký kết hiệu hóa học: là tên gọi viết tắt của một nguyên tố chất hóa học trong bảng tuần hoàn hóa học.
7. Biện pháp nhớ bảng tuần hoàn những nguyên tố hóa học
7.1. Ghi ghi nhớ bảng tuần hoàn hóa học bằng phương pháp truyền thống
Nhận biết các thành phần của từng nguyên tố: Khi áp dụng bảng tuần trả hóa học, chúng ta đọc phải ghi nhận được số nguyên tử, nguyên tử khối trung bình, thông số kỹ thuật electron, độ âm điện, số oxi hóa, thương hiệu nguyên tố, ký hiệu hóa học. Tất cả đều phải sở hữu trong ô thành phần của bảng tuần hoàn.
Học vài nguyên tố mỗi ngày: Đây là một trong những cách học được rất nhiều học sinh áp dụng. Đối cùng với bảng tuần hoàn có nhiều nguyên tố khó khăn nhớ với các thông số thì vấn đề phân nhỏ tuổi ra để học nó góp não ghi ghi nhớ được một bí quyết lâu dài.
Dán các bảng tuần hoàn chất hóa học tại địa điểm dễ chú ý thấy
Làm thẻ ghi chú cho mỗi nguyên tố. Phương pháp làm này y hệt như làm một tập flashcard.
7.2. Dùng cách thức ghi ghi nhớ bảng tuần trả hóa học
7.2.1. Theo dãy vận động hóa học tập của kim loạiChắc hẳn bạn nào thì cũng nhớ một lời nói quen thuộc: “Khi nào nên may áo giáp sắt lưu giữ sang phố hỏi siêu thị Á Phi Âu”. Đây là câu nói để ghi ghi nhớ 16 nguyên tố hóa học trong dãy chuyển động hóa học tập của kim loại. Dãy hoạt động hóa học tập của sắt kẽm kim loại bao gồm: Na, F, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au.
7.2.2. Theo bài bác ca hóa trịViệc ghi nhớ theo bài ca hóa trị cũng là 1 trong cách ghi lưu giữ bảng tuần hoàn hóa học. Những em học sinh có thế xem thêm bài ca hóa trị sau đây nhé!
Trên đây là toàn cục những định hướng cơ phiên bản cần nắm rõ về bảng tuần hoàn hóa học. Để rất có thể làm giỏi bài tập, những em bắt buộc nắm chắc và ghi ghi nhớ bảng tuần trả này. Muốn ôn thi đạt được công dụng tốt, các em học tập sinh hoàn toàn có thể truy cập tức thì vào căn cơ học online q6.edu.vn để hoàn toàn có thể đăng ký tài khoản hoặc liên hệ nhanh qua trung tâm cung cấp của q6.edu.vn để ôn tập được thiệt nhiều kỹ năng nhé!














